ザイゴマインプラントに関連した論文
本日紹介する論文は、

~はじめに~
今回ご紹介するのは2023年にMedicina Oral Patología Oral y Cirugia Bucalにて報告されたこちらの論文です。インプラント周囲の軟組織の減少を頬脂肪体を用いて防ぐことができるかについて、パイロット研究ではありますが、明らかにした論文です。現在All-on-Xやザイゴマインプラントをしている先生で、インプラント体周囲の軟組織の減少に悩まれている先生方だけではなく、これからザイゴマインプラントを始められる先生方にもリカバリー方法の一つとして知っていただければ幸いです。
~背景~
骨再生材料を用いた複雑な口腔外科手術は、骨吸収過程の治療に用いられてきた。しかしながら、長期間無歯顎であった患者における重度上顎萎縮の管理は、未だ歯科医療における課題である。
1990年にザイゴマインプラントおよびその外科手技が初めて報告されて以来、本術式は患者の罹患率ならびに治療費用および治療期間を短縮することを目的として改良されてきた。一部の著者は、ザイゴマインプラントの生存率は従来型インプラントと同等であり、99.5%を上回ると指摘している。
それにもかかわらず、ザイゴマインプラントにはいくつかの合併症が存在し、最も頻度が高いのはインプラント周囲軟組織の問題である。平均プロービングデプスが6 mmを超え、プロービング時出血の有病率が45%に達することが報告されている。
軟組織の変化は病原性細菌の存在と関連するとされているが、微生物が存在しない場合でも、これらのインプラントにおいてプロービングデプスが増大していたことが示されている。これに関連して、副鼻腔外経路で埋入されたザイゴマインプラントでは、インプラント体が口腔粘膜組織と密接に接触しているため、露出したインプラント体に起因してインプラント周囲の炎症が生じ、続いて軟組織退縮が生じる可能性がある。
頬脂肪体は、さまざまな種類の口腔・顎顔面領域の合併症の管理に用いられてきた。一部の著者は、ザイゴマインプラント手術の際に頬脂肪体を利用しており、15か月以上の経過観察期間において術後およびインプラントに関連する合併症が認められなかったと報告している。
本研究の目的は、頬脂肪体を用いることがインプラント体周囲の軟組織退縮を予防し得るかどうかを評価することであった。すなわち、本研究では、頬脂肪体が口腔粘膜の厚みを増加させ得ることから、ザイゴマインプラントの露出部位を頬脂肪体で被覆することにより、将来的なインプラント周囲軟組織の退縮を予防できるかどうかという仮説を検証することを目的とした。
〜材料と方法〜
― 研究デザイン(Study design)
本研究は、各ザイゴマ骨に2本ずつのインプラント治療を必要とする患者を対象とした、パイロット、前向き、単盲検、スプリットマウス、無作為化臨床試験として実施した。被験者は、術後72時間、7日、15日、3か月、6か月、12か月時点でフォローアップを行った。本試験は2013年ヘルシンキ宣言に準拠して実施され、Clínico San Carlos Hospital の倫理委員会による承認(19/531-R_P)を受けた。
― 参加者(Participants)
参加者は、マドリード・コンプルテンセ大学口腔外科大学院クリニックで実施された研究プロジェクトを通じて募集した。登録された患者はすべて18歳以上であり、アメリカ麻酔科学会(ASA)分類に基づく外科的リスクがASA IまたはASA IIであった。さらに、コーンビームCTにより残存上顎骨が4 mm未満と測定され、各頬骨に2本のザイゴマインプラントによる治療が必要と判断された患者を対象とした。すべての参加者には研究内容について詳細な説明を行い、文書による同意を得たうえで登録した。
― 外科手技(Surgical procedure)
患者は、ベンゾジアゼピン系薬剤(ミダゾラム 1 mg/ml, Anesfarma, Spain)による静脈内意識下鎮静と、アドレナリン0.1 mg/ml含有塩酸アーティカインによる局所麻酔(Ultracain 40 mg, Normon, Spain)を併用して治療を受けた。外科処置は、30年以上の臨床経験を有する高熟練の口腔顎顔面外科医(J.L-Q.)により施行された。すべてのザイゴマインプラントは、1回の手術セッションで埋入した。
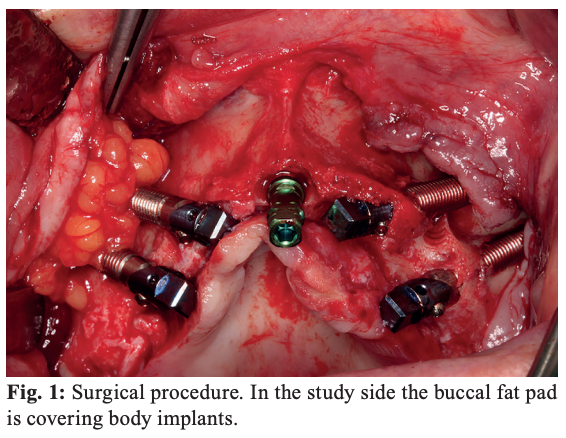
さらに、各被験者は2つの研究群の両方に割り付けられた。2本のザイゴマインプラント埋入後に被覆弁のみを縫合する対照群(A群)と、インプラント埋入後、露出したインプラント体の骨外部分を覆うように頬脂肪体を再配置し(Fig.1)、その後に弁を縫合する実験群(B群)である。両群におけるそれ以前の外科手技は同一であり、術者はドリルシークエンスシステムに従い、HE Zygomatic Implant Neodent®(Straumann AG, Basel, Switzerland)を埋入した。すべてのザイゴマインプラントを埋入後、各インプラントはZAGA分類システムに従って分類した。
術後薬物療法として、オメプラゾール20 mg(Kern Pharma, Madrid, Spain)を1日1回20日間、Augmentin 875/125 mg(GSK, GlaxoSmithKline, Brentford, U.K.)を8時間毎に1回15日間、Deflazacort 30 mg(Laboratorios Menarini S.A., Naples, Italy)を1日2回5日間、Dexketoprofen 25 mg(Laboratorios Menarini S.A., Naples, Italy)を8時間毎に1回5日間、Metamizole 575 mg(Laboratorio Stada S.L., Barcelona, Spain)を8時間毎に1回3日間投与した。
さらに、オキシメタゾリン 0.5 mg/ml 点鼻スプレーを片側鼻腔に1日3回3日間、フルチカゾンフランカルボン酸エステルを1日2噴霧15日間、ならびに生理食塩水(GSK, GlaxoSmithKline, Brentford, U.K.)による鼻腔洗浄を併用した。
― アウトカム評価項目(Outcome measures)
主要評価項目は、両群間におけるインプラント周囲軟組織厚の差とした。これは、インプラントプラットフォーム頬側の3か所における測定値の平均を、歯周プローブ(HH12 periodontal probe, Deppeler SA)を用いて記録することにより算出した。
副次評価項目は以下のとおりである。
疼痛はVisual Analog Scale(VAS)を用いて評価し、腫脹はAmin & Laskin法、血腫はGutiérrez y Wuesthoff法に従って評価した。副鼻腔炎はHwang質問票を用いて評価し、インプラント生存率はAparicioの成功基準に従って判定した。
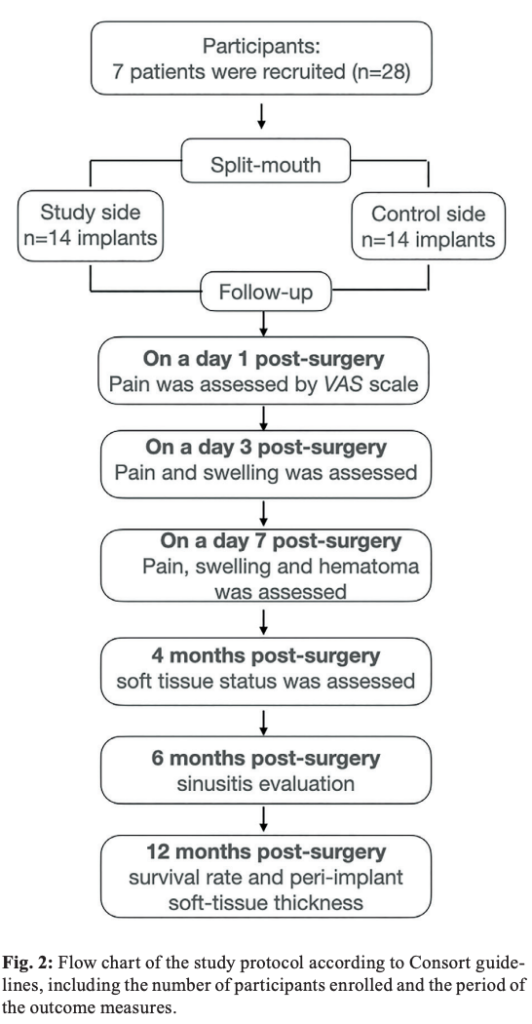
すべての評価項目は、訓練を受けた独立した非盲検評価者(S.B.R)により測定された(Fig. 2)。
― サンプルサイズ、無作為化手順および統計解析(Sample size, randomized sequence, and statistical analysis)
本研究はパイロットスタディであるため、サンプルサイズの算出は行わず、7名の患者を登録した。したがって、合計28本のザイゴマインプラントを統計単位として解析対象とした。
被験者の無作為化は、Matlab 28b(MathWorks, Natick, Massachusetts, USA)を用いた単純無作為化法により実施した。統計解析としては、記述統計を中央値・分散および百分率を用いて行った。さらに、Shapiro–Wilk検定を用いてデータの正規性を評価し、仮説検定にはノンパラメトリック検定であるWilcoxon検定を用いた。
〜結果〜
12か月のフォローアップ後、7名の患者において合計28本のザイゴマインプラントを評価した(女性71%、男性29%)。参加者の平均年齢は55.57±6.39歳であり、平均手術時間は172.14±54.60分であった(Table 1)。
Shapiro–Wilk検定により、両群における疼痛データは正規分布に従うことが確認された。しかし、腫脹の分布は標準化された基準を満たさなかったため、両臨床指標についてノンパラメトリック検定(Wilcoxon検定)を用いて評価した。
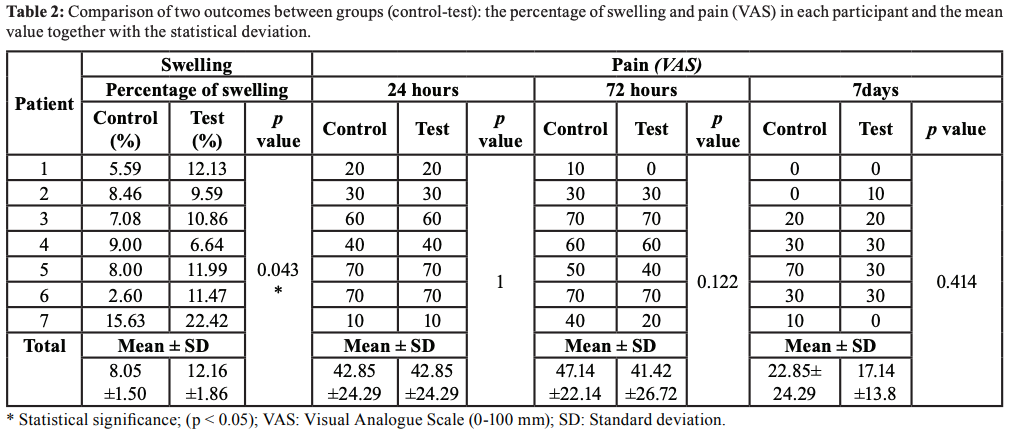
腫脹に関するアウトカムでは、両群間に統計学的有意差が認められた(p=0.043)。具体的には、実験群における腫脹の平均割合は12.16%であり、対照群の8.05%と比較して高値を示した。さらに、実験群で記録された腫脹の最大割合は22.42%であり、対照群の15.63%よりも6.79%高かった。腫脹および疼痛の結果はTable 2に示す。
3名の患者に血腫が認められ、いずれも両側性に発生した。しかしながら、実験群では影響を受けた顔面部位の数がより多かった。さらに、実験群では、すべての検査側半顔において頬部に血腫が認められたのに対し、対照群では3例中1例のみに同部位で観察された。対照側の1例では、術後5日目に縫合部離開が生じた(14.28%)。一方、治療から6か月後、対照群の1名に副鼻腔炎および眼窩周囲皮膚瘻が認められた。
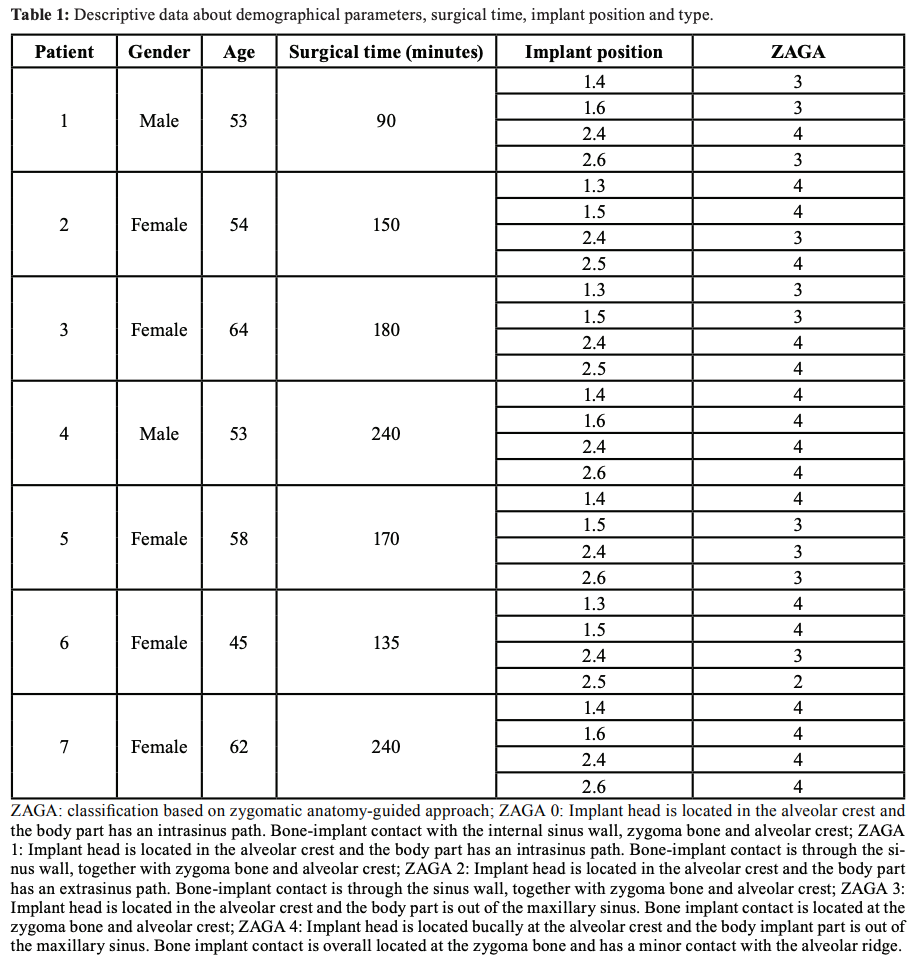
インプラント周囲軟組織厚は、フォローアップに来院しなかった2名を除き、28本中20本のインプラントにおいて評価した。実験群の平均値は5.2±1.47 mmであり、対照群の3±1.05 mmと比較して有意に大きかった(p=0.03)。対照群では、インプラントの14.3%において10 mmの粘膜裂開が認められたが、実験群ではいずれのインプラントにも認められなかった。これらの結果はTable 3に示す。