ザイゴマインプラントに関連した論文
本日紹介する論文は、

~はじめに~
今回ご紹介するのは2023年9月に Dentistry Journalにて報告されたこちらの論文です。ザイゴマインプラント支持補綴におけるメンテナンスおよび合併症の早期介入を目的とした体系的プロトコールを提案した論文です。フォローアップ期間中の生物学的および技術的状態を包括的に評価でき、軟組織変化や咬合咬耗の早期発見が可能になると思われますので、これからザイゴマインプラントを用いた治療をされる先生方は勿論、メンテナンスで悩まれている先生方には是非読んで頂きたい論文です。
1.緒言
ザイゴマインプラントは、上顎に高度な骨萎縮を有する患者の治療において、近年ますます使用されるようになっている。本手法は、従来のインプラント治療と同等の成功率を示している一方で、一定の外科的熟練を要し、また合併症のリスクを伴うことも報告されている[1,2]。
ザイゴマインプラントは、無歯顎で高度に萎縮した上顎の治療[3–6]や、上顎切除後欠損の再建[7]において有効な治療選択肢であることが示されてきた。これらのインプラントは、腫瘍切除、外傷、先天異常などにより広範な上顎欠損を生じた患者の補綴的リハビリテーションを目的として、Brånemark により導入された[8]。頬骨弓の骨を長いインプラントの確実な支持基盤として利用し、従来型インプラントと併用することで、エピテーゼ、補綴装置、あるいはオブチュレーターの固定源として機能させるという革新的なアプローチであった。この方法は、患者の機能回復および審美性の改善に大きく寄与し、社会生活における自信と日常性の回復を可能にしてきた。
インプラント治療の長期的成功および合併症予防において、適切なメンテナンスは不可欠である。2017年のワールドワークショップにおいて、Renvert らは歯科インプラントにおける「健康」の定義について報告している[9]。しかしながら、ザイゴマインプラントは、インプラントの長さ、傾斜、位置、上顎洞や眼窩など他の解剖学的構造との関係、歯槽頂部における骨の欠如または減少、補綴装置の設計といった点で従来型インプラントとは大きく異なっており、従来の検査・評価アプローチを適用することが困難である。
最近のシステマティックレビューでは、ザイゴマインプラント支持補綴における最も一般的な合併症として、軟組織裂開、副鼻腔炎、補綴装置の破折が挙げられている[4]。さらに、メンテナンス中には、重度の歯肉過形成/肥厚、褥瘡、瘻孔、水平的歯肉裂溝などが観察されることもある。Aparicio らは2006年に、メンテナンスプログラムの一環として副鼻腔の健康状態を評価する必要性を提唱している[10]。
軟組織の変化は細菌性粘膜炎のリスクを高める可能性があり、その予防および管理はインプラント周囲炎を防止するうえで極めて重要である[11]。フルアーチのインプラント支持補綴においては、プラークの蓄積とインプラント周囲炎との直接的関連は明確に示されていないものの[12,13]、ザイゴマインプラントに関する微生物学的研究では、プロービング時の出血と歯周病原性細菌との関連が報告されている[14]。
ザイゴマインプラントは、標準的な口腔内インプラントとは異なるインプラント周囲解剖学的特徴を有する。すなわち、インプラントの頬側部分は多くの場合軟組織のみに囲まれており、口蓋側骨が欠如していることも少なくない。インプラントの安定性は主に頬骨内に埋入された先端部によって得られるためである。このような特徴により、歯科インプラントに通常用いられる歯周評価指標を適用することは困難であり、デスモゾーム結合を損なわないよう、慎重なプロービング手技が求められる。Agliardi らによる2017年の前向き研究では、プロービングは軟組織の良好な付着を確認し、合併症を予防する目的でのみ用いるべきであると示唆されている[15]。
さらに、インプラントの立ち上がり位置が歯槽頂から頬側または口蓋側に逸脱していることが多く、粘膜ヒダの形成、付着歯肉の欠如、頻繁な口蓋側配置などにより、補綴装置装着下での診査、プロービング、清掃操作は困難となる。それでもなお、ザイゴマインプラント周囲のプロービングは難易度が高いものの、インプラント周囲組織炎症を早期に察知するための有用な臨床行為の一つである。
Aparicio らによれば、既存文献におけるザイゴマインプラントの治療成績および合併症の報告は一貫性に乏しく、標準化された体系的評価が欠如している。特に、ザイゴマインプラント治療における成功度や治療リスクを明確に定義するための基準が不足している点が指摘されている。また、健全な歯槽骨に埋入された従来型インプラントと同一の評価基準でザイゴマインプラントを評価する傾向が依然として存在する。しかし、ザイゴマインプラントは、生体力学、臨床プロトコール、治療成績、さらには合併症の様相において従来型インプラントとは本質的に異なっている。これらのインプラントは歯槽骨および基底骨の吸収変化と関連しており、従来の評価基準では治療結果を適切に表現できない[16]。
インプラント・補綴治療を一体として捉えると、補綴構造物の詳細な観察も不可欠であり、破折線や異常咬耗を早期に検出し、補綴医に報告する必要がある。また、咬合変化や患者が訴える疼痛を把握するため、顎関節(TMJ)の診査も定期的に実施すべきである。2020年には、Aparicio によりザイゴマ成功コードが改訂され、ORIS 成功基準が更新された[16]。これに基づき、ザイゴマインプラントの評価は以下の5段階に分類される。
成功条件1:すべての成功基準を満たし、最適な状態にある。
成功条件2:軽微な変化は認められるが、臨床的影響はない。
成功条件3:臨床的に変化が認められる境界的状態であるが、適切な治療により長期的維持が可能である。
条件4:補綴装置を支持している生存インプラントであるが、提案された評価基準による測定が行われていない。
条件5:インプラントの失敗を示し、介入または再治療を要する。
最良の治療成績を得るためには、これらの基準に基づきザイゴマインプラントを包括的に評価し、治療中に生じ得る問題を早期に特定することが重要である。しかしながら、合併症を予防することを目的としたザイゴマインプラントの検査ガイドラインは、現在のところ文献上に存在しない。本論文は、ザイゴマインプラントのメンテナンスおよび合併症の早期介入に関するガイドラインを提示する初の報告であり、ORISスケールにおけるステージ2および3の患者を早期に識別することを目的としている。本研究では、重度骨萎縮を有し、ザイゴマインプラントによる高度なインプラント・補綴リハビリテーションを受けた患者を対象に、生物学的および技術的合併症の予防または早期発見のために有用な口腔内・口腔外診査手技および機器について詳述する。
2. 材料および機器
本研究で提案するプロトコールは、ザイゴマインプラント支持による固定式補綴治療を対象としており、ザイゴマインプラントを用いた補綴リハビリテーションおよびメンテナンスにおいて200名以上の患者を治療してきた著者らの臨床経験に基づいて構築されたものである。
各フォローアップ診察時には、まず臨床医が、補綴装置装着後に取得された診療録および画像診断資料(X線画像等)を慎重に確認する必要がある。これにより、連結されているインプラントの本数、位置、接続様式、トランスミューコーザルパスの走行、ならびに補綴装置の適合状態および設計を把握することが可能となる。
この種の補綴治療においては、インプラント埋入後かつ補綴装置未装着の状態で撮影した口腔内写真を体系的に保存し、将来の診査時における比較評価のためのベースライン資料として用いることが望ましい。
また、各フォローアップ診察において、口腔内および口腔外診査を行う前に、臨床医は患者への問診を実施し、補綴治療に対する満足度の評価、症状の有無の確認、ならびに口腔衛生指導への遵守状況を把握する必要がある。
3. 詳細手順
インプラント埋入後、24時間以内に暫間的なフルアーチのスクリュー固定式補綴装置が装着される。著者らは、特に手術時に広範な組織剥離を伴うことが多い点を考慮すると、骨および軟組織の安定化を図るため、術後最初の4か月間は暫間補綴装置が必要であると考えている。
外科的縫合は術後2週間で抜糸され、治癒期間中は、0.12~1%クロルヘキシジンジグルコン酸塩を含有するゲル状歯磨剤を用いた超軟毛歯ブラシの使用、および粘膜組織の治癒促進を目的としたヒアルロン酸配合のジェルまたは洗口液の使用を患者に指導する[17]。
暫間補綴期間中は、少なくとも月1回のフォローアップを行うことが推奨される。
術後4か月時に画像検査による評価を行い、最終印象採得後、最終補綴装置を装着する。最終的なインプラント支持補綴装置は、プラークの蓄積を防止し、患者自身による口腔清掃が可能であり、かつ臨床的評価を行いやすい設計とする必要がある。
術後1年間は、歯科衛生士による4回のメンテナンス来院を設定することが推奨される。最終補綴装置装着後1か月目の初回歯科衛生士来院時には、患者に対して適切な口腔清掃およびメンテナンス方法の指導を行うとともに、本論文で提案する5段階プロトコールに基づいた診査を開始する。この初回診査は、患者の不十分な清掃に起因する合併症を予防するとともに、専門的介入を要する問題を早期に発見するうえで極めて重要であり、これらの詳細は以下の5ステップで述べる。
この点は、全顎補綴および高度骨萎縮を有する患者において特に重要である。このような患者は、過去に不十分な口腔ケアや不良な清掃習慣により多数歯を喪失していることが多く、喫煙者であったり、手指の巧緻性が低下している場合も少なくない。さらに、フルアーチ補綴構造は天然歯の解剖学的形態とは異なり、ボリュームが大きく清掃が困難であり、特に舌側および口蓋側領域では清掃性が著しく低下する。そのため、集中的な再教育プログラムが必要となる。
これらのフルアーチ補綴再建においては、重度の粘膜炎、強い炎症、インプラント周囲炎、排膿、腫脹、または技術的合併症が認められる場合を除き、専門的口腔清掃のために補綴装置を撤去することは避けることが推奨される。そのため、最終補綴装置装着前に、補綴装置全体および内面(インタリオサーフェス)の写真を撮影しておくことが望ましい。これにより、歯科衛生士が補綴装置と粘膜との境界部の清掃方法を適切に指導することが可能となる。実際、凹面形態や長いフランジは清掃アクセスを妨げ、バイオフィルムの蓄積を助長する可能性がある。
さらに、Aparicio らの提案に基づき、術後1年目および以降5年ごとにCBCT撮影を行い、上顎洞の評価を行うことが推奨される。副鼻腔評価には、鼻副鼻腔炎研究のためにタスクフォースが推奨するLund–Mackay分類が有用であり[18]、これは妥当性が検証されたスコアリングシステムである。この画像評価は、前篩骨洞、後篩骨洞、上顎洞、前頭洞、蝶形骨洞、および骨膜口複合体の6領域を対象とし、それぞれに0、1、または2点が付与される。0点を超えるスコアが認められた場合、異常(陽性)所見と判断される。
ザイゴマインプラントによる補綴治療においては、Malevez らが指摘するように、口内法X線写真は有用な情報を提供しない場合が多い[19]。これは主に、①萎縮した上顎では口蓋部の湾曲が減少していること、②ザイゴマインプラントが通常傾斜した角度で埋入されること、の2点に起因する。さらに、インプラントのヘッド部や一部のボディが残存歯槽突起の外側、あるいは前上顎壁の外に位置する場合、インプラント全周が骨に囲まれていないこともある。このような状況では、辺縁骨高の測定によってインプラント成功を評価することは意味をなさない。なぜなら、インプラントは意図的に骨外に配置されているためである。
本論文で提案するザイゴマインプラント患者のフォローアップおよびメンテナンスプロトコールは、以下に示す5つのステップから構成されており、最終補綴装置装着後(すなわち術後約4か月以降)のメンテナンス期に適用することが推奨される。
3.1 ステップ1:口腔内・口腔外および顎関節(TMJ)の診査
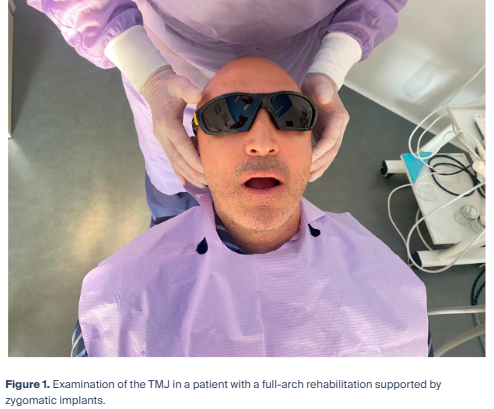
第1ステップでは、口腔内および口腔外の軟組織ならびに顎関節の診査を行う。臨床医は、顎関節におけるクリック音や関連痛の有無を確認する必要がある(図1)。これは、特にフルアーチ即時荷重プロトコールによって治療された患者において、補綴的垂直的顎間距離が大きく変化している場合に重要である。
顎関節症状が認められる場合には、咬合バランスの精査に加え、咬筋活動および心拍を同時に記録可能な携帯型ホルターモニターを用いた筋電図検査によるブラキシズムの評価が推奨される。ブラキシズムが確認された場合には、ナイトガードの使用が推奨される。
続くステップでは、顔面および頸部リンパ節の触診(図2a)ならびに副鼻腔に対する口腔外からの指による打診(図2b)を行い、インプラント周囲および副鼻腔内における炎症過程の早期徴候を検出することを目的とする。
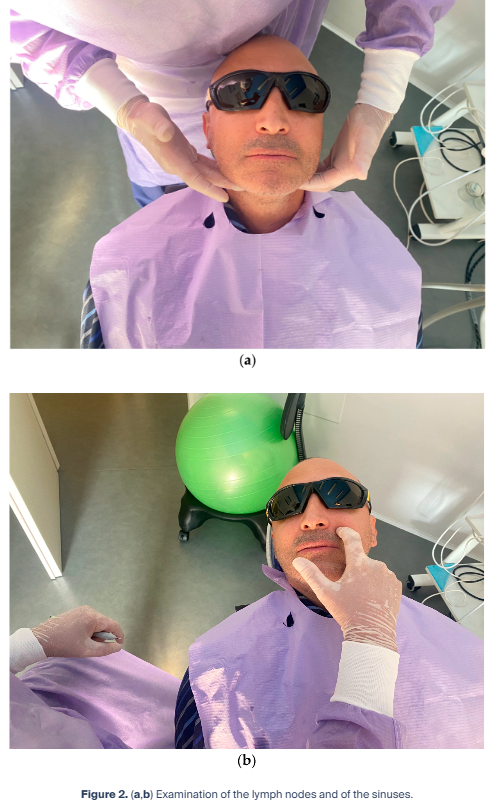
また、患者からの申告、あるいは術者が感知した持続性の口臭についても記録することが推奨される。この段階は、鼻副鼻腔炎(rhinosinusitis)を診断するうえで特に重要である。Lanza と Kennedy[20]が示したように、鼻副鼻腔炎の診断には主要基準および副次基準が存在する。主要基準には、顔面痛または圧迫感、顔面のうっ血または膨満感、鼻閉、膿性分泌物、嗅覚低下または嗅覚消失、診査時に認められる膿性所見、発熱が含まれる。一方、副次基準には、頭痛、発熱(急性期以外)、口臭、倦怠感、歯痛、咳嗽、耳痛、耳閉感が含まれる。これらの基準に基づき、主要基準が2項目以上、または主要基準1項目と副次基準2項目以上が認められた場合に、鼻副鼻腔炎と診断される。
3.2 ステップ2:軟組織およびトランスミューコーザルパスの観察
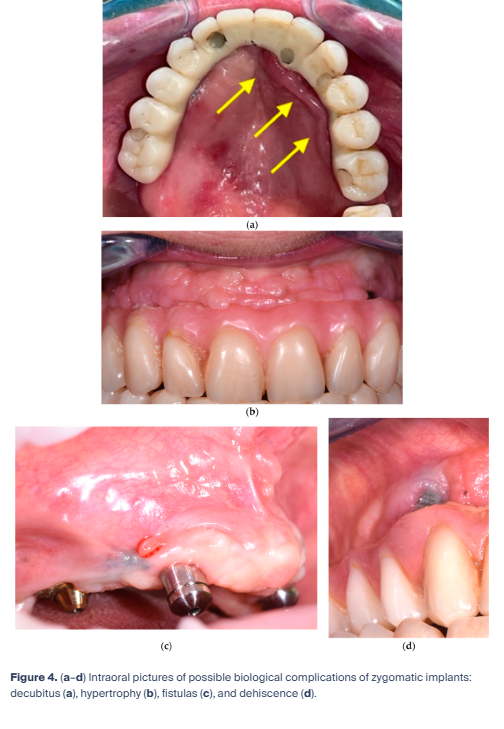
第2ステップでは、インプラントおよび補綴装置周囲の軟組織を診査する。この段階では、トランスミューコーザル部の褥瘡(図4a)、開窓(フェネストレーション)、肥厚(図4b)、瘻孔(図4c)、および裂開(図4d)を同定し、記録する必要がある。
これらの所見が認められた場合には、補綴装置をスクリューで撤去し、インプラント周囲組織の状態および補綴フレームワークの形態を評価する。また、歯肉と補綴装置との間隙が不十分であることによる清掃困難の有無についても検討を行う。
本段階で使用する器具としては、リトラクター(例:Optragate®, Ivoclar Vivadent, Schaan, Liechtenstein)、ガーゼ、および拡大視野用光学ルーペが挙げられる。
3.3 ステップ3:インプラント周囲指標および組織のデジタル刺激
従来型歯科インプラントにおいては、最新のガイドラインにより、インプラント周囲プロービングは、歯槽頂部骨吸収の評価およびインプラント周囲の健康状態または疾患状態を判定するために必須の臨床手技と定義されている[21]。しかしながら、頬側に歯槽頂骨が存在しないエクストラサイナス型ザイゴマインプラントにおいては、同一の評価基準を適用することはできない。
さらに、ザイゴマインプラントでは、標準的な基準値の欠如、粘膜の肥厚、補綴装置のボリューム、ならびにアングルドアバットメントの使用といった要因により、トランスミューコーザルパスを歯周プローブで評価すること自体が困難であり、プロービングによる歯槽頂骨のモニタリングは不可能である。
一方で、この種のインプラントにおいても、プローブの使用は、出血の有無および粘膜シールの健康状態を臨床的に評価する目的で有用である。プローブの挿入角度は、インプラント周囲のデスモゾーム性シールを破壊し、口腔―上顎洞交通を引き起こす可能性を回避するため、従来の45°よりも大きな角度とする必要がある[7]。
評価に際しては、柔軟性を有する非金属製の歯周プローブを用い、0.25 N の軽圧で慎重なプロービングを行う(図5a)。これにより、粘膜シールの状態を確認するとともに、プラーク指数(PI)、プロービング時出血(BoP)、および排膿の有無を記録する。
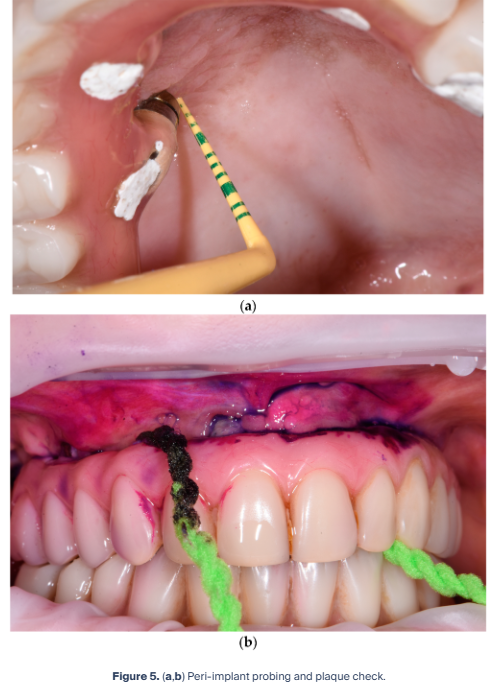
補綴装置およびインプラント上のプラーク沈着は、プラーク染色液を用いることで検出し、患者に視覚的に提示することが可能である(図5b)。ただし、アクリルレジン製補綴装置を対象とする場合には、低研磨度のエアポリッシングシステム(<65 µm)が使用可能な場合に限り、プラーク染色液の使用が推奨される。これらが利用できない場合、染色液の除去が困難となる可能性がある。
本ステップで使用する器具は、非金属製の柔軟なプローブ、プラーク検出剤、スポンジ状デンタルフロス、および光学拡大装置である。
3.4 ステップ4:補綴装置の検査
インプラント支持補綴装置の機能開始後1年以内に機械的問題を検出することは、オッセオインテグレーションを損なう可能性のある生体力学的合併症や、インプラント周囲粘膜の炎症を防止する上で極めて重要である。この期間に患者を管理する医療従事者は、補綴学的異常を識別できる専門的知識を有し、異常が認められた場合には速やかに専門医へ報告することが求められる。
この観点から、第4ステップでは、補綴構造物の検査を行い、咬耗(図6a)、チッピング(図6a)、破折線(図6b)、水平的および垂直的動揺(図6c)、ならびに清掃性(清掃アクセス)の確保状況(図6d)を評価する。咬合異常が認められた場合には、まず対合歯列を評価し、その後インプラント補綴装置を撤去して咬合器上で再装着し、咀嚼運動を再評価する。チッピングが認められた場合には修理を行い、必要に応じて口蓋側金属補強を追加する。
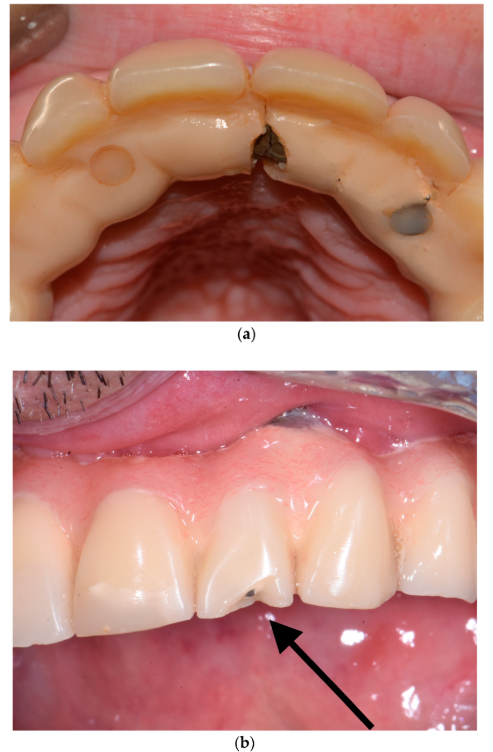
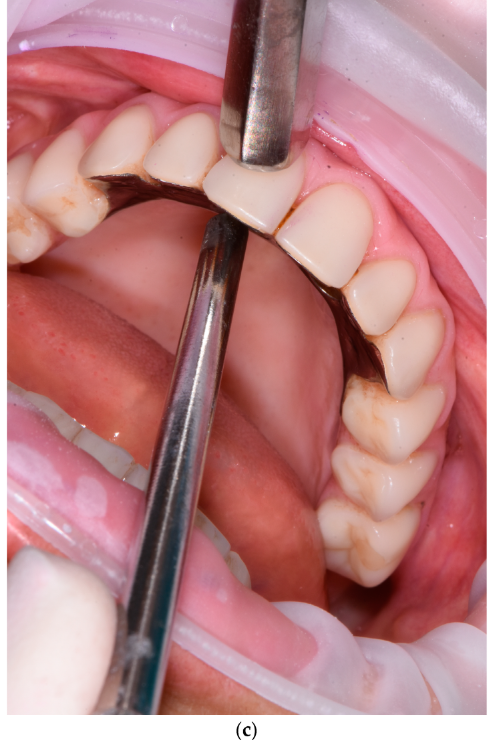
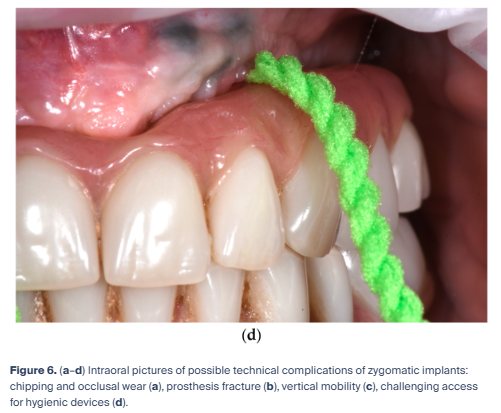
本ステップで使用する器具は、スポンジ状デンタルフロスおよび光学拡大装置である。
3.5 ステップ5:写真記録
最後に推奨されるステップは、少なくとも年1回、口腔内および口腔外写真を撮影・記録し、粘膜裂開(デヒセンス), 咬耗, およびその他の合併症の進行状況を経時的にモニタリングすることである。
4. 考察
著者らの知る限り、本論文はザイゴマインプラントによって補綴治療を受けた患者のメンテナンスに関するガイドラインを提示し、その診査プロトコルを提案した初めての報告である。これに類似する報告としては、Aparicio ら[16]による研究が挙げられ、同研究ではザイゴマインプラント支持補綴の成功を評価するための ORIS 基準が提示されている。Aparicio の論文の目的は、従来型インプラントおよびザイゴマインプラントの双方に用いられてきた成功基準を検証し、ザイゴマインプラント補綴の治療成績を評価するための、より明確な基準を示した 改訂版ザイゴマ・サクセスコードを提示することであった。
過去30年以上にわたり、重度に顎堤が吸収した患者の口腔リハビリテーションにおいて、インプラント埋入前または同時の骨移植は標準的な治療法とされてきた。しかし、関連する多くの報告が存在する一方で、上顎洞底挙上術の有効性についてはいまだ議論の余地がある[7]。これらの手技を扱った既存文献の多くでは、インプラントの成功および失敗を定義する明確な基準が示されておらず、初期骨高の測定値や標準化されたX線学的フォローアップデータが十分に提示されていない場合が多い[7]。最近発表された後ろ向き研究では、外側法による上顎洞底挙上術と同時に埋入されたインプラントの累積生存率(CSR)は、10年で95%、20年で85%であったと報告されている[22]。一方、システマティックレビューでは、ザイゴマインプラントのCSRは12年で95.21%と報告されている[23]。
ザイゴマインプラントの最終的な目的は、重度に障害された上顎を有する患者において、咀嚼機能、審美性、快適性を回復させ、自己肯定感および社会的自信を向上させることにある。インプラント支持固定性補綴装置はこれらの目的を効果的に達成し、結果として高い患者満足度および高い治療成功率につながる[24]。生活の質(QOL)や患者満足度を評価した研究では、前歯部に通常のインプラントを、後方部にザイゴマインプラントを併用した固定性補綴による無歯顎性萎縮上顎のリハビリテーションが、患者のQOLおよび治療満足度を有意に向上させたことが報告されている[24]。
本稿では、ザイゴマインプラントに関連する課題および起こり得る合併症を明らかにし、それらを予防するために厳密なメンテナンスプロトコルの遵守と、口腔内外組織の多角的な評価が重要であることを強調している。
本研究で提案した5ステッププロトコルは、合併症の早期発見およびザイゴマインプラントを有する患者の健康維持を目的としている。メンテナンス中に歯科衛生士が異常を察知した場合には、速やかに外科医へ症例を報告し、必要な診査および介入を行うことが重要である。
本論文は、長期予後および患者満足度の向上を目的とした、専門的および在宅メンテナンスのための臨床プロトコル確立に向けた予備的報告である。従来型インプラント支持によるフルアーチ固定性補綴装置に対しては、専門的および在宅口腔衛生管理のための器具やプロトコルが提案されている[25]が、ザイゴマインプラントでは、周囲軟組織の特性や補綴装置の形態的特徴により、同様の手技が適用できない場合がある。
例えば、エアポリッシング装置は、補綴装置を撤去しない状態でもフルアーチ固定性補綴装置の専門的清掃に有効であることが示されているが、ザイゴマインプラントにおいては、繊細な軟組織シール構造や周囲の重要な口腔外解剖構造との近接性を考慮すると、適切に使用されなければ安全性が確保できない可能性がある。そのため、ザイゴマインプラントに特化した使用ガイドラインの策定が必要である。
また、本プロトコルの一部は翼突(プテリゴイド)インプラントの評価にも応用可能である。翼突インプラントは、ザイゴマインプラントと比較して低侵襲であり[26]、上顎結節および口蓋骨錐体突起を貫通して蝶形骨翼突突起に固定されるため、通常のインプラントよりも長いインプラントが使用される[27]。All-on-4コンセプトと併用することで、各上顎臼歯部に翼突インプラントを配置し、遠心カンチレバーを不要とすることが可能となり、補綴設計に起因する合併症を軽減しつつ、完全なフルアーチリハビリテーションが実現される。
近年の計量書誌学的研究において、Ramal-Sanchez は1990年から2021年までに「zygomatic implants」をキーワードとして発表された論文を分析し、本分野における専門家間の協力と知識共有の重要性を強調している。このような協働は、治療の標準化を促進し、患者のQOL向上および合併症の低減に大きく寄与する[28]。
ザイゴマインプラント治療における臨床的成功および合併症発生率の低減には、外科的および補綴的なラーニングカーブの克服だけでは不十分であり、適切かつ専門的なメンテナンスプログラムとの併用が不可欠である。これには、外科医、補綴歯科医、歯科衛生士、歯科技工士を含む歯科医療チーム全体の緊密な連携が求められる。
結論として、本論文は、ザイゴマインプラントによる補綴治療を受けた患者を適切に診査し、インプラント支持補綴の予後を損なう可能性のある合併症を早期に検出するためのガイドラインを提示することを目的としている。今後の研究では、本リハビリテーションの維持に適した専門的口腔衛生プロトコルの検討が求められる。